J. Pharm. Anal. 期刊社论:CLDN18.2靶向分子成像
 2023年8月,北京大学肿瘤医院杨志主任、朱华研究员团队、和北京工业大学高学云教授受邀在药学领域TOP期刊《Journal of Pharmaceutical Analysis》(医学1区/药学1区,JCR Q1)撰写有关“CLDN18.2靶向分子成像与GI肿瘤的精准治疗”展望的社论。曾在北京大学肿瘤医院联合培养的陈艳博士研究生(2023年7月毕业于贵州大学,目前就读于北京工业大学)为本文第一作者。
2023年8月,北京大学肿瘤医院杨志主任、朱华研究员团队、和北京工业大学高学云教授受邀在药学领域TOP期刊《Journal of Pharmaceutical Analysis》(医学1区/药学1区,JCR Q1)撰写有关“CLDN18.2靶向分子成像与GI肿瘤的精准治疗”展望的社论。曾在北京大学肿瘤医院联合培养的陈艳博士研究生(2023年7月毕业于贵州大学,目前就读于北京工业大学)为本文第一作者。
今年3月,创胜集团与北京大学肿瘤医院朱华教授团队合作,在期刊《Journal of Pharmaceutical Analysis》上发表用于胃肠道肿瘤无创成像的靶向CLDN18.2免疫PET探针[89Zr]Zr-DFO-TST001的研究结果。
论文链接(点击文末左下角“阅读原文”可直接跳转):https://www.sciencedirect.com/science/article/pii/S2095177923000357

Claudin18.2(CLDN18.2)是一种通常只表达于正常胃黏膜细胞的紧密连接蛋白。当恶性肿瘤发生时,细胞极性丢失,细胞间黏附结构被破坏,CLDN18.2因此暴露在肿瘤细胞表面。CLDN18.2在约40%的人表皮生长因子受体2(HER2)阴性胃肠道癌症中特异性表达,这使其成为一个有前景的新兴治疗靶点。正如最近报道的那样,靶向CLDN18.2抗体zolbetuximab在CLDN18.2阳性和HER2阴性胃癌患者中显示出惊人的疗效。在临床实践中,CLDN18.2表达状态的评估对于患者治疗方案的制定十分关键。分子成像可作为非侵入性的检测手段用于疾病的诊断、分期和疗效监测。已有CLDN18.2的分子成像结果陆续被发表,CLDN18.2分子探针的开发对肿瘤靶向治疗的发展具有重要意义(下图)。
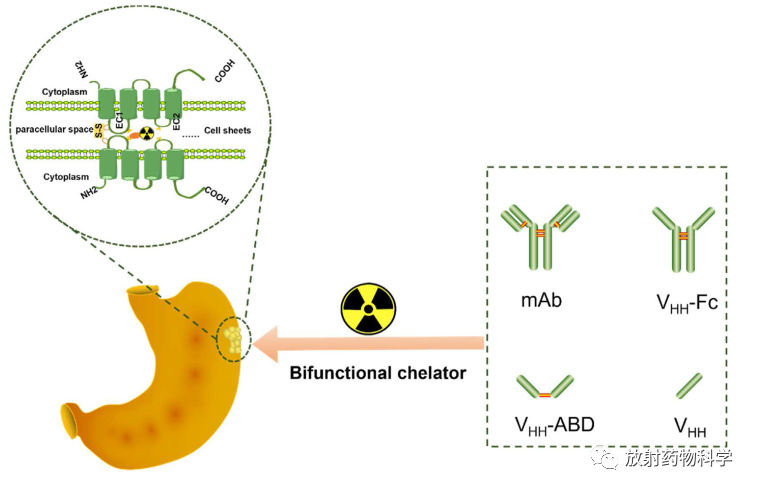
1.CLDN18.2表达状态检测的意义
近年来,已有多个靶向CLDN18.2的单克隆抗体、抗体-偶联药物(ADC)和嵌合抗原受体-T(CAR-T)疗法用于临床研究。CLDN18.2特异性单抗Zolbetuximab在SPOTLIGHT和GLOW研究均取得了阳性结果,表明Zolbetuximab单抗联合化疗治疗CLDN18.2高表达胃癌患者比单一化疗具有更显著的生存获益。此外,一些早期的研究已经对该靶点的其他单克隆抗体和ADC药物进行了评估,也展现出良好的应用前景。FAST研究表明, Zolbetuximab单抗联合化疗可提高CLDN18.2高表达患者的无进展生存期和总生存期。
因此, CLDN18.2表达状态是筛选具有CLDN18.2靶向治疗潜在获益患者的先决条件,但准确测定其表达水平仍是现在面临的诸多挑战之一。不同检测方法的蛋白质表达的临界值不同,即使是同一患者的同一标本,不同检测方法的检测结果也不同,给临床带来很大的困难。免疫组织化学是一种有创性的离体检测方法,胃癌具有高度异质性,因此难以实时动态反映患者所有病灶的CLDN18.2表达状况。
2.用于病灶非侵入性检测的功能性分子成像
核医学分子影像探针利用放射性示踪剂发出的放射性信号检测靶标蛋白在病灶中的表达和分布,可以评估靶向治疗的疗效和预后,从而指导肿瘤的准确诊断和治疗。基于CLDN18.2的功能分子探针的PET成像可以获得肿瘤患者全身病灶的CLDN18.2表达信息以及肿瘤对CLDN18.2靶向药物的响应。此外,探针的开发也可能用于未来药物不良反应的研究,有研究表明,未既往胃切除术的患者在接受Zolbetuximab单抗治疗时比既往胃切除术的患者更容易发生呕吐。可能的原因是CLDN18.2单克隆抗体非特异性识别了正常胃粘膜细胞上的CLDN18.2抗原表位,导致胃粘膜损伤。因此,或许可以利用CLDN18.2靶向分子探针来可视化CLDN18.2单克隆抗体在肿瘤和胃黏膜中的摄取,为其毒性研究提供影像学参考。我们最初使用124I标记了鼠源单克隆抗体5C9进行临床前研究,结果表明该探针可以定位和指导CLDN18.2阳性肿瘤的手术。不仅如此,还构建了近红外荧光II成像探针FD 1080-5C9,这两种示踪剂为癌症的功能成像和手术指导提供了一种实用的分子成像策略,但还需要进一步的临床验证。随后,本课题组又开展了124I标记的人源化抗体18B10 (10L)的0期临床试验,结果显示124I-18B10 (10L)可以通过PET功能成像反映CLDN18.2过表达的肿瘤病变。然而,成像过程中患者需要继续服用碘来阻断甲状腺对碘-124的生理摄取,要求患者具有高度的依从性。基于GMP级别CLDN18.2靶向TST001单抗的[89Zr]Zr-DFO-TST001探针也用于胃肠道肿瘤中CLDN18.2表达水平的初步检测,为CLDN18.2治疗提供了可行的目标患者筛选和疗效评估方法。
3.CLDN18.2及其他免疫治疗的功能分子成像研究进展
众所周知,探针是功能成像的“灵魂”。即使是基于GMP级别的TST001的放射性探针也在肝脏和脾脏具有较高的非特异性摄取,其原因可能是全抗的Fc段与肝脏中的Fc受体的非特异性结合,或许在未来可进行抗体工程化修饰以降低其在肝脏中的高背景摄取。此外,可以开发更小的尺寸的探针,例如基于Fab、纳米抗体、亲和体和肽的CLDN18.2靶向探针。较小的分子具有更强的肿瘤组织穿透力和更快的血液清除率。CLDN18.2功能分子探针的构建原则应该是:在保留肿瘤特异性和亲和性的同时,最大限度地减少非靶器官和组织的摄取,提高成像的对比度,为CLDN18.2靶向放射性药物的研发和肿瘤精准诊疗一体化奠定基础。
设备必不可少。除了核素分子探针的研发,核医学分子影像在疾病诊疗中的快速发展也离不开影像设备的升级换代。PET成像检查与代谢相关,为病理生理学提供了一种量化方法。然而,目前临床上广泛应用的静态PET采集设备每次测量仅产生单个累积图像。传统的PET成像只关注定性而非定量评估。在给患者静脉注射放射性药物后,通常需要等待一段时间才能获得图像,这段时间用于放射性示踪剂在感兴趣的器官中积聚,以及从非靶器官中洗出。然而,放射性药物的分布是一个动态的过程,其分布肿瘤和正常器官之间,以及患者之间都有很大的差异。传统动态PET采集通常是单床位,这使得扫描仪轴向的覆盖范围受到限制。得益于行业技术的持续发展,临床动态全身(DWB) PET成像的新框架已经出现,早期的PET系统需要延长扫描持续时间以获得足够的计数统计数据,而DWB-PET系统可以在相当短的持续时间内达到与静态检测器系统相同的图像质量。在动态图像中的单个体素级别生成不同的动力学数据,能够通过动力学建模生成参数化图像。
然而,CLDN18.2功能性分子探针作为放射性药物CLDN18.2在临床上的应用也面临诸多挑战。放射性药物的安全应用涉及医用回旋加速器、符合GMP的放射性药物制造设施和符合相关辐射安全标准的专用治疗场所。因此,至建立可靠的分销网络至关重要,以确保安全和及时地运送这些药物。与常规癌症治疗药物相比,放射性药物的生产周期和物流(输送、应用和管理)时间还必须根据放射性核素的半衰期进行调整。
临床需求是从分子成像到靶向治疗的最终目标。放射性核素药物偶联物(RDC)类似于ADC,其通过具有靶向性的抗体/Fab或小分子(包括亲和体或肽)介导的定位来精确破坏病灶,以避免全身辐射暴露的潜在危险。区别在于RDC有效载荷是放射性核素(如2+和-核素),具有诊断和治疗功能。在配体选择方面,根据肿瘤靶向性和药代动力学特征可尝试不同分子大小的靶向分子。基于CLDN18.2靶向分子探针在CLDN18.2阳性肿瘤中的高特异性和亲和力,可以利用治疗性核素177Lu对胃癌进行放射性核素治疗。
总之,CLDN18.2靶向药物在各大临床研究中显示出了显著疗效。借助全身PET成像设备的动态成像能力,CLDN18.2功能分子探针有望实现在体内无创准确检测CLDN18.2阳性病变,在疗效评估、预后、多靶点共表达人群治疗、联合免疫治疗等方面也具有应用前景。


参考文献:
Yan Chen, Zhi Yang, Xueyun Gao, Hua Zhu. CLDN18.2-targeted molecular imaging and precision therapy of gastrointestinal tumors, Journal of Pharmaceutical Analysis, 2023,ISSN 2095-1779, https://doi.org/10.1016/j.jpha.2023.08.007.
(https://www.sciencedirect.com/science/article/pii/S2095177923001971)




